Axelle SCOIZEC1, Rozenn SOUILLARD1, Rodolphe THOMAS1, Sophie LE BOUQUIN1
1Ebeac, Anses-Ploufragan.
Début janvier 2017, une première mission a été menée par des équipes de l’unité d’épidémiologie aviaire de l’Anses de Ploufragan (Ebeac) dans des foyers déclarés d’influenza aviaire hautement pathogène (IAHP) ou des élevages fortement suspects dans les départements des Landes et du Gers. Via la réalisation de prélèvements supplémentaires à ceux réalisés par les DDPP à des fins de gestion, l’objectif de la mission était la collecte d’informations sur les virus IA circulants (en particulier les virus IAHP H5N8 ou H5Nx apparentés aux H5N8) afin d'évaluer la contamination environnementale et mieux connaître la dynamique d'infection dans les élevages.
Méthodologie
Chaque atelier enquêté appartenait à un élevage officiellement confirmé infecté mais le statut de chaque atelier n’était pas systématiquement connu au moment de l’enquête. En effet, un élevage pouvant comporter plusieurs ateliers distincts de volailles, les ateliers peuplés appartenant à un même foyer (détecté sur les résultats d’analyse d’un atelier cas index) peuvent ne pas être tous infectés au même moment.
Pour chaque atelier enquêté (atelier infecté ou suspect, non dépeuplé et avant mise en œuvre de toute mesure de nettoyage/désinfection), il était prévu de prélever 30 animaux par prise de sang, écouvillon trachéal et écouvillon cloacal, de collecter les commémoratifs concernant la mortalité et l’expression clinique de la maladie, et de réaliser des prélèvements environnementaux dans le bâtiment et sur le parcours selon un protocole standardisé. Au total, sept exploitations (confirmées officiellement infectées par un virus H5HP apparenté aux virus H5N8 de clade 2.3.4.4 circulants actuellement en Europe) ont été visitées et douze ateliers de canards (prêts à gaver ou reproducteurs) ont été prélevés : dix ateliers avec réalisation de prélèvements sur les animaux et neuf avec réalisation de prélèvements environnementaux. De plus, des prélèvements environnementaux ont été effectués dans la zone périphérique des foyers visités dans des sites jugés d’intérêt : proximité de parcours de lots infectés, zones humides à proximité, route d’accès aux foyers…
Résultats
Résultats concernant les animaux des ateliers enquêtés
Parmi les dix ateliers dont les animaux ont été prélevés, huit ont été détectés infectés (c’est-à-dire que le lot était positif à la recherche virologique par RT-PCR temps réel gène H5).
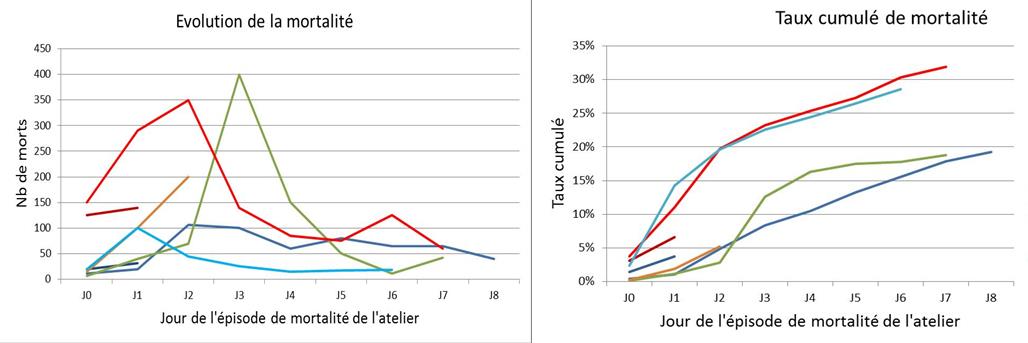
Les résultats des analyses réalisées sur les animaux montrent une séroconversion massive sur sept des huit lots infectés : pour ces sept lots infectés, la proportion d’animaux séropositifs vis-à-vis d’un antigène H5N8 (représentatif des souches IA H5HP clade 2.3.4.4 circulant actuellement en Europe) variait de 90 à 100 %. La séroconversion peut être précoce par rapport à l’apparition de la mortalité : un lot avec 100 % des animaux prélevés ayant séroconverti présentait de la mortalité depuis une journée. Au sein des huit lots infectés, la proportion d’animaux positifs en RT-PCR temps réel gène M variait de 31 à 100 % et celle en gène H5 de 15 à 100 %. Ces lots présentaient une mortalité depuis une durée variant de un à dix jours. Pour les sept lots pour lesquels des commémoratifs détaillés étaient disponibles, l’évolution de la mortalité, présentée dans la figure 1, se caractérisait schématiquement par une augmentation très forte pendant deux à trois jours suivie d’une diminution progressive. Sept à huit jours après le début de la mortalité, la mortalité cumulée variait entre 19 et 32 %. Certains éleveurs signalaient le début de signes cliniques deux à trois jours avant l’apparition de la mortalité. Les symptômes étaient au début un simple abattement, avec des animaux apathiques, sans notification de baisse de consommation d’aliment ou d’eau. Les signes ensuite observés étaient nerveux et locomoteurs (titubation, torticolis, animaux tournant en rond, difficulté à se déplacer) et étaient concomitants au démarrage de la mortalité. La durée d’incubation observée peut être estimée entre six à huit jours d’après la cinétique d’apparition des signes cliniques entre les ateliers au sein des mêmes foyers.
Figure 1 : Evolution de la mortalité dans les ateliers infectés*, jusqu’au jour de prélèvement
(7 ateliers avec commémoratifs de mortalité jour par jour)
* 5 ateliers confirmés officiellement infectés par un virus H5HPN8, et 2 ateliers avec expression clinique, RT-PCR H5 positive dans des foyers confirmés officiellement H5HPN8.
Les variations constatées dans l’excrétion virale, la séroconversion et l’évolution de la mortalité entre les lots infectés semblent indiquer que la dynamique d’excrétion au sein d’un lot peut très probablement varier selon plusieurs paramètres (condition d’élevage, état sanitaire, âge des animaux au moment de la contamination,…), et également que l’apparition de la mortalité par rapport à l’évolution de l’infection au sein d’un lot peut sans doute varier sensiblement d’un lot à l’autre. Les données collectées permettent également de penser que, dans certains ateliers, si l’épisode d’influenza aviaire allait à son terme, entre 60 et 80% des canards d’un lot de prêts à gaver pourraient survivre à un épisode clinique d’infection par un virus apparenté aux virus H5N8 circulant actuellement en Europe (clade 2.3.4.4).
Résultats concernant l’environnement des ateliers infectés
Des prélèvements sur l’environnement ont été réalisés dans huit ateliers détectés infectés (deux confirmés infectés par les prélèvements officiels, et six avec des prélèvements positifs en virologie par RT-PCR gène H5 lors de cette étude) et dans un atelier non détecté infecté. Pour chacun de ces huit ateliers détectés infectés, des prélèvements réalisés dans les bâtiments étaient positifs en RT-PCR temps réel gène H5, ce à la fois pour les ateliers dans lesquels le lot était en démarrage de phase de mortalité (1 jour ou 2 jours après le début de la mortalité) comme pour ceux dont le début de la mortalité datait de plus de six jours. Les bâtiments présentaient une forte contamination que ce soit en termes de fréquence de détection et de résultats précoces1 en RT-PCR temps réel : sur mangeoires et abreuvoirs (dans tous les ateliers pour lesquels ces prélèvements ont été réalisés : respectivement 7/7 et 6/6), sur sol, litière, murs et entrées/sorties d’air (dans quasiment tous les ateliers infectés pour lesquels ces prélèvements ont été réalisés : de 5/6 à 7/8). On détecte également du génome viral par PCR jusque dans le sas plus de la moitié des ateliers infectés pour lesquels ces prélèvements ont été réalisés (soit 5/8). Tous les prélèvements étaient négatifs dans l’atelier avec un lot non détecté infecté. Ce qui tend à confirmer que la détection de génome viral dans les bâtiments des ateliers infectés est bien liée à l’excrétion virale par les lots infectés.
Les parcours ayant été utilisés par les lots trouvés infectés présentent des résultats positifs en RT-PCR temps réel gène H5 pour quatre des cinq ateliers concernés. Au moment des prélèvements, les parcours étaient vides d’animaux depuis six à sept jours pour quatre d’entre eux (trois PCR positifs et un PCR négatif) et depuis un jour seulement pour le dernier (PCR positif). Sur les parcours, les points majeurs de détection de génome viral sont la zone de sortie des animaux du bâtiment et les déjections sur parcours, et dans une moindre mesure les zones humides, les abreuvoirs et les mangeoires. Un cas intéressant concerne un parcours dont des prélèvements se sont révélés positifs en RT-PCR temps réel gène H5 alors que les animaux étaient claustrés depuis sept jours et ne présentaient de la mortalité que depuis un jour : sous réserve que le lot infecté soit bien à l'origine de cette contamination, cette détection pose la question d’une excrétion très précoce par rapport à l’apparition de la mortalité (infection éventuellement asymptomatique avec excrétion virale de certains animaux), la question d’une contamination aéroportée à courte distance et celle du rôle des vecteurs indirects (il s’agit ici de canards PAG « confinés » en tunnel semi ouvert sur l’extérieur).
Pour une exploitation infectée, la route de sortie, dans le périmètre de l’exploitation, a été prélevée et s’est révélée positive par RT-PCR temps réel gène H5. Cela pose la question de la diffusion indirecte à courte distance via les personnes, les véhicules ou autres vecteurs.
Même si la mise en évidence du génome viral (RT-PCR temps réel) dans l’environnement ne permet pas de statuer sur la viabilité (capacité infectieuse) des virus ainsi détectés, celle-ci témoigne néanmoins que du matériel viral y a été déposé en quantité détectable.
Résultats concernant l’environnement autour des exploitations infectées
Sur les 26 prélèvements réalisés dans l’environnement autour des exploitations infectées (proximité de parcours infectés, lac ou étang fréquenté par l’avifaune sauvage et à proximité de foyers, route à proximité de foyers), trois prélèvements ont été trouvés positifs en RT-PCR temps réel gène M mais la suite des analyses n’a pas permis de mettre en évidence le gène H5 par RT-PCR temps réel sur ces échantillons : sur une bande entre 1 à 2 m à l’extérieur d’un parcours et sur des fientes fraiches d’oiseaux sauvages. Les résultats semblent donc montrer que l’environnement autour des foyers n’est pas fortement contaminé, même si ces résultats méritent d'être pris avec précaution compte tenu de l’échantillonnage restreint (en surface et nombre points prélevés) sur ces zones. Cela peut expliquer en partie le fait que les élevages de galliformes présents dans les zones infectées soient moins touchés que les élevages de canards. En effet, d’après des études menées aux USA avec les virus H5N8 y circulant en 2014-2015 (Bertran et al., 2016 ; Pantin-Jackwood et al., 2016), la réceptivité des espèces galliformes est inférieure à celle des palmipèdes. Les doses de virus diffusées à faible distance pourraient être insuffisantes pour contaminer des galliformes au contraire des palmipèdes, sachant que d'autres facteurs peuvent expliquer la moindre transmission aux galliformes, en particulier, le rôle d'une transmission indirecte au sein de la filière de palmipèdes par mouvements d'animaux, véhicules et personnes (avis de l'Anses 2017-SA-0026).
Autres éléments épidémiologiques
Les ateliers infectés prélevés sont pour plusieurs d’entre eux situés dans une même zone avec une forte densité d’élevage de palmipèdes et dans laquelle la grande majorité des élevages de palmipèdes ont été détectés infectés par IAHP H5N8. La diffusion de proche en proche semble donc la voie de diffusion du virus à l’échelle de cette micro zone. Dans cette zone, la plupart des foyers sont à moins de 500 m d’un autre foyer. L’un des foyers prélevés est par exemple situé à moins de 500 m de trois autres foyers confirmés. La diffusion de proche en proche peut être due à une diffusion à courte distance via des vecteurs indirects (personnes, véhicules, faune domestique, faune sauvage). La voie aéroportée ne peut pas être exclue à ce stade. Les éleveurs enquêtés ont signalé dans la gestion des foyers, des facteurs, ne concernant pas des mesures réglementaires mais ayant pu favoriser la diffusion à courte distance du virus via les personnes et les véhicules : maintien de mouvements de véhicules et de personnes à proximité des foyers détectés, délai de plus d’une semaine avant l’abattage des animaux même lorsque le confinement de ceux-ci est limité. La difficulté de restreindre le passage de véhicules et de personnes devant les élevages infectés (mesure non réglementaire), ainsi que les délais dans le dépeuplement des foyers, sont en en lien avec la densité élevée d'élevages et le nombre élevé de foyers et ont dû contribuer à la diffusion du virus.
Conclusions
Malgré le faible nombre d’ateliers inclus dans cette étude (12), les résultats obtenus dans les dix ateliers infectés présentant des manifestations cliniques sont dans l’ensemble concordants et permettent une première évaluation de la contamination environnementale de ceux-ci et de la dynamique de l’infection au sein de ces lots.
On détecte du génome viral dans l'environnement à la fois dans les bâtiments et sur la plupart des parcours des ateliers infectés. La présence de génome viral ne signifie pas que le virus est viable mais signale que du matériel viral est présent en quantité détectable. La détection du génome viral sur ces parcours peut perdurer au moins sept jours après le vide d’animaux (dans les conditions météorologiques rencontrées : froides et humides). La contamination environnementale apparaît être très importante à l’intérieur des bâtiments. Une contamination de l’environnement autour des élevages apparaît plus faible mais a été mise en évidence en pourtour de parcours et sur une route en limite d’exploitation dans un foyer.
Les résultats des analyses réalisées sur les canards des lots infectés ainsi que la contamination importante de l’environnement et ce même au moment du démarrage de l’épisode clinique, indiquent qu’une excrétion massive et une circulation rapide du virus sur l’ensemble de la bande ont très certainement lieu plusieurs jours avant le démarrage de la mortalité. Ceci est un facteur favorisant avant détection de l’infection, la diffusion du virus via les personnes, les véhicules et tout autre vecteur mécanique (avifaune, matériel, etc.).
Dans les foyers inclus dans l’étude, les délais de plus d’une semaine pour l’abattage des lots et les difficultés pour restreindre le passage des véhicules et des personnes devant les élevages infectés (mesure non réglementaire), qui s’expliquent notamment le nombre élevé de foyers au moment de leur détection et par la densité élevée d’élevages, ont dû contribuer à la diffusion du virus. Ceci est d’autant plus probable que la fréquence de détection de génome viral dans l’environnement des foyers démontre que celui-ci a été largement contaminé, et que la proportion d’animaux excréteurs au sein des lots est important et peut perdurer plus de dix jours après le début de la phase clinique sur un lot.
L’importance et les caractéristiques de la contamination environnementale mises en évidence par ces premières investigations, ainsi que les résultats des investigations complémentaires à venir, sont et seront des éléments qui pourront nourrir un retour d’expérience sur le modèle de contrôle de la diffusion de l’infection entre élevages
Remerciements aux éleveurs ayant accepté de participer à cette étude, aux directions départementales de protection des populations des Landes et du Gers pour leur appui et aux Laboratoires des Pyrénées et des Landes pour la réalisation des analyses et leur disponibilité.
Remerciements aux relecteurs : le Laboratoire national de référence de Ploufragan, la coordination Plateforme.
Bibliographie
Bertran, K., Swayne, D.E., Pantin-Jackwood, M.J., Kapczynski, D.R., Spackman, E., Suarez, D.L.
Lack of chicken adaptation of newly emergent Eurasian H5N8 and reassortant H5N2 high pathogenicity avian influenza viruses in the U.S. is consistent with restricted poultry outbreaks in the Pacific flyway during 2014-2015 (2016) Virology, 494, p. 190-197.
Pantin-Jackwood, M.J., Costa-Hurtado, M., Shepherd, E., DeJesus, E., Smith, D., Spackman, E., Kapczynski, D.R., Suarez, D.L., Stallknecht, D.E., Swayne, D.E.
Pathogenicity and transmission of H5 and H7 highly pathogenic avian influenza viruses in mallards (2016) Journal of Virology, 90 (21), p. 9967-9982.
1Une présence importante d’ARN d’influenza aviaire dans l’échantillon aboutira à un résultat en RT-PCR temps réel qualifié de précoce ; à l’inverse une présence faible d’ARN IA dans l’échantillon aboutira à un résultat qualifié de tardif. A noter que ces notions de « précoce » et « tardif » sont indépendantes de la précocité de l'infection chez l'animal.